0.5ml의 압달라 백신은 근육 내 주입을 위한 중단제로 준비된 사스-CoV-2 바이러스의 수용체 결합 부위(RBG)를 함유한 50mcg의 재조합 단백질 백신을 포함하고 있다.
보건부는 2021년 9월 17일자 4471/QD-BYT 결정을 발표했는데, 이는 코비드-19 질병 예방 및 통제의 긴급한 요구에 대한 압달라 백신의 조건부 승인에 관한 것이다.
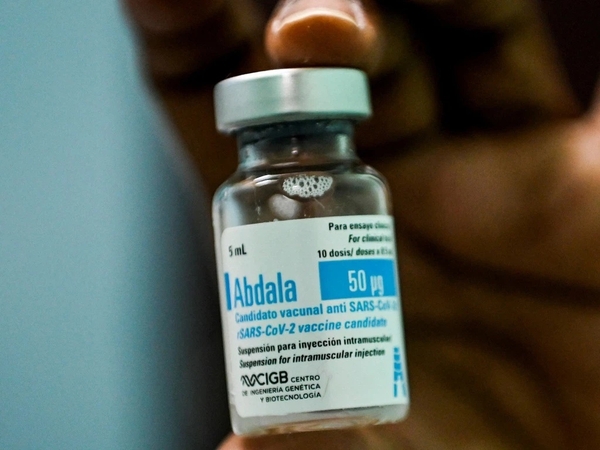
*압달라 백신
압달라 백신은 정부 2012년 5월 8일자 약사법 제54조 2017년/ND-CP 제67조의 규정에 따라 승인되었다.
승인 문서에 따르면 이 백신은 AICA Raberaties Company, BBU(Base Business Unit) AICA-쿠바에서 제조된다. 그리고 반제품으로 수출되어 쿠바 유전공학 및 생명공학 대학(CIGB)의 레벨 2에서 포장되었다.
베트남에서는 백신 및 의료생물의 연구생산센터(POLYVAC)가 이 백신의 승인을 요청했다.
보건부는 또한 코비드-19 전염병의 예방과 통제에 있어 긴급한 필요성에 대한 압달라의 승인에 첨부된 조건들을 명시하고 있다.
각 백신 투여량은 근육 내 주입을 위한 중단제로 준비된 사스-CoV-2 바이러스의 수용체 결합 부위(RBG)를 함유한 재조합 단백질 백신 50mcg를 포함하고 있다. 백신은 10개의 병으로 된 상자에 포장되어 있으며, 각각 10회 복용량, 0.5ml씩 들어 있다.
CIGB가 발표한 정보에 따르면 압달라 백신은 임상 3상의 결과는 코비드-19 환자의 사망을 예방하는 데 100% 효과적인 것으로 나타났다.
전에 압달라는 증상을 보이는 코비드-19 전염을 예방하는 데 92.28% 효과적이라고 보고되었다.
앞서 베트남은 아스트라제네카(아스트라제네카 생산), 스푸트니크V(가말레야 연구소), 코비드-19 얀센 백신(존슨앤존슨), 스파이크박스(코비드-19 백신 모더나), 코미르나티(화이자바이오앤텍), 베로셀(중국 국립 바이오텍 그룹(CNBG)/Sinopharm) 및 Hayat-Vax 등 7개의 백신을 긴급 사용 허가했다.